18015531058

GMP净化车间:
GMP的目标是确保建立科学的、严格的无菌药品生产环境、工艺、运行和管理体系,较大限度地消除所有可能的、潜在的生物活性、灰尘、热原污染,生产出高品质的、卫生安全的药物产品。我们所说的生物制药净化工程-GMP洁净厂房工程解决方案和污染控制技术就是保证GMP成功实施的的主要手段之一。
全国服务热线:18915730122 在线咨询
GMP标准
生物制药企业要求GMP的目标是确保建立科学的、严格的无菌药品生产环境、工艺、运行和管理体系,较大限度地消除所有可能的、潜在的生物活性、灰尘、热原污染,生产出高品质的、卫生安全的药物产品。我们所说的生物制药净化工程-GMP洁净厂房工程解决方案和污染控制技术就是保证GMP成功实施的的主要手段之一。
通过对生物制药客户生产环境的深入研究和工程经验积累,清阳清楚了解生物制药生产过程环境控制的关键;
节能是清阳净化系统方案优先考虑的重点;
清阳擅长的就是给予客户符合GMP及Fed 209D, ISO14644, IEST, EN1822国际标准要求,同时应用新的节能技术的环境解决方案;
清阳净化可以提供从GMP整厂规划设计——人流物流净化方案、洁净空调系统、洁净装饰系统;整厂节能改造、水电、超纯气体管道、洁净室监测、维护系统等全面安装配套服务;
GMP洁净车间净化参数:
换气次数:100000级≥15次;10000级≥20次;1000≥30次。
压差:主车间对相邻房间≥5Pa;
平均风速:10级、100级0.3-0.5m/s;
温度 冬季>16℃;夏季 <26℃;波动±2℃。
湿度45-65%;
GMP粉剂车间湿度在50%左右为宜;
电子车间湿度略高以免产生静电;
噪声≤65dB(A);
新风补充量是总送风量的10%-30%;
照度300LX
GMP净化车间设计依据:
1)<药品生产质量管理规范>(卫生部1992年修订);
2)<医药工业洁净厂房设计规范>(1997年)
3)<药品生产管理规范()实施指南>(1992)
4)<洁净厂房设计规范>(1984)
5)<采暖通风与空气调节设计规范>(GBJ19-87)
6)<无菌医疗器具生产管理规范>(YY/T-0033-90)
7)甲方提供的工艺平面布置图等有关技术资料;
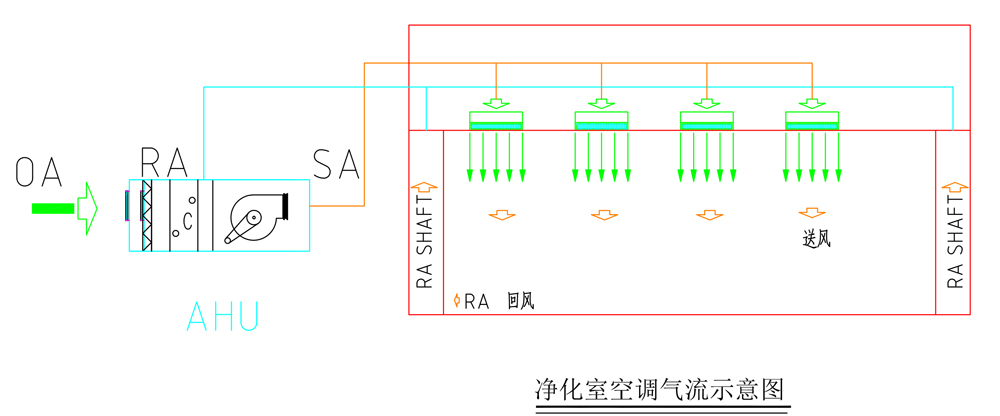
GMP净化车间的建设原理:
净化车间的工作原理主要通过空气过滤来实现。一般要经过初效过滤、中效过滤、高效过滤三个阶段。
气流经初效净化进入加湿段→加热段→表冷段→中效净化→风机送风→管道→高效净化风口→吹入房间→带走尘埃细菌等颗粒→回风百叶窗→初效净化,经过这一系列过程,即可达到净化目的。
GMP净化车间的建筑材料选择:
1.净化厂房墙、顶板材一般多采用50mm厚的夹芯彩钢板制造,其特点为美观、刚性强。
2.圆弧墙角、门、窗框等一般采用专用氧化铝型材制造。
3.地面可采用环氧自流平地坪或高级耐磨塑料地板,有防静电要求的,可选用防静电型。(关于无尘净化车间装修施工的地板材料,如需详细了解,还可点击此处获取无尘净化车间装修施工之地板材料)。
4.送回风管道用热镀锌板制成,贴净化保温效果好的阻燃型PF发泡塑胶板;高效送风口用不锈钢框架,美观清洁,冲孔网板用烤漆铝板,不生锈不粘尘,宜清洁。
药品GMP净化车间的结构:
针对医疗医药类GMP车间,应根据生产产品的类别来确定整体结构。
1. 医药针剂生产:由于其主要生产设备均用生产联动线,所以对厂房的长宽都有要求,钢筋混凝土结构的厂房不太实用,以砖墙结构为佳。
2. 固体药剂生产:生产单元步骤相对独立,建议利用厂房原有分隔布置(前提是结合设备情况,事先安排好设备的进场安装及维修路线)。
在洁净室建设或改建时,不能依赖于最终的竣工验收来保证洁净室的质量,必须从设计及设备选型阶段就严格把关,在建设的全过程中对主要关键点严格检查、监督,在实际使用中定期监测才能保证洁净室达到设计指标和使用要求.无菌医疗器械是任何标明“无菌”的医疗器械,生产洁净室是保证无菌医疗器械质量的基本条件,控制无菌医疗器械生产过程的环境并规范其生产,防止环境对无菌医疗器械污染,洁净室必须满足规定环境参数的要求来建设和定期监测。
清阳医疗器械GMP无尘车间装修工程覆盖:一类/二类/三类医疗器械,医药,试剂等各行业医疗药品保健食品GMP等车间装修工程;
清阳医疗器械GMP无尘车间洁净等级涵盖:十万级,万级,千级,百级,十级等洁净等级,A级,B级,C级,D级各等级无菌超净间装饰装修工程;
清阳医疗器械GMP净化工程项目覆盖范围有上海,江苏,浙江,安徽,湖北等多地,累积超过30万平无菌厂房面积,300多家企业选择清阳工程;
清阳客户80%回头率&75%转介绍率,为各行业业主提供净化厂房装修服务,价格1步到位!
清阳工程17年专业净化装修资质+消防资质+机电安装,打造的无尘车间平稳运行15年无压力;


清阳工程不仅仅是无尘车间的施工方,更是为您企业安心投产的保险方!
消防设施工程专业承包2级、建筑装修装饰工程专业承包2级、建筑机电安装工程专业承包2级资质;



工程管理团队 专业管理团队+专业施工人员,持证上岗


工程细节&隐蔽工程 规范施工,隐蔽工程细节处拒绝敷衍了事


无尘车间装修早知道,选择净化工程公司方法(避免入坑)
①、不知道怎么着净化工程公司报价?---一定要有资质!专业净化工程公司都有机电安装资质;
②、对无尘车间施工一无所知?----先结合行业标准与企业自身实际需求定方案;
③、对无尘车间质保及售后服务不了解?不知道规避风险?----避免中间商转包带来的沟通服务不便;
④、对工程所用的主要材料有哪些不清楚,对其质量及品牌不放心?----按预算,选择相应价位品牌;结合日后维护与节能方面;
⑤、核心设备后续维护是否便捷?----清阳为您从设计开始,从使用寿命与维护便捷入手选材;
⑥、洁净不达标,GMP验收不合格----清阳洁净度可以达到或者超过要求标准交付,很多公司洁净度不达标多次找清阳给解决案;
⑦、工程建设行业乱象---价格低恶性竞争拿下项目,方案没从客户实际需求做详细或特意漏项,后面靠增项收取费;
---清阳可以免费提供无尘车间设计方案:价格及细则一目了然,解决您的所有困扰 ---
【资质】清阳具备国家住建部签发的机电三级资质,施工二级资质,安全生产许可证,网上可查询;
【经验】17年服务经验,做过超过百家设计电子,医疗,生物,制药,精密机械,食品,化妆品等多个行业;
【专业】拥有自己设计及施工团队,含有电工,焊工,起重工等多特种技工,持证上岗,专人负责;多个先进测试设备,为需要认证的净化项目保驾护航;
【口碑】我司成立于2007年,至此300多个项目实操经验,诚信守法;
【价格】我们拥有自己的净化产品生产线,价格优势游于很多同行;



17年优胜劣汰选择供应商-清阳坚信-材料和设备决定工程品质

①在核心净化设备上除采用品牌空调,清阳工程自有净化设备研发团队及工厂,自主研发生产新型FFU高效过滤器;

清阳掌握净化核心,让洁净更节能 !更为您省电费
②地坪及墙板工程,清阳工程经过多年的筛选,选用的材料材质经得起时间的检验;让您的车间耐用,美观大气!


欢迎微信咨询客服;工程服务热线:18915730122

掌握核芯,必达标
公司自有净化核心产品初中高效过滤器产线,产品自己研发及生产,减少核心部件的不稳定性,保障洁净度,使用寿命长,运营成本更低!
免费勘查,合理设计
现场免费勘查,根据需求设计,可出合理的结解决方案
17年精选供应商
精选知名频卖设备及材料供应商,让项目工程高质量完成,诚信经营,性价比高,工期有保障
有证·专业,团队才有底气
专业工程师证书,施工人员持证上岗,电工证、焊工证、起重工证等证书齐全
1对1项目跟踪管理,施工有保障
严格执行国家标准,符合建筑规范,做良心工程,杜绝隐患;采用1对1项目管理,保障施工现场全程服务;

---江浙沪皖8小时到现场勘查,24小时出设计方案 ---
清阳净化谨以专业、专注、专心、品质、节能为生存格言自成立之日起一直在洁净领域努力探索积累,
我们在行业的定位-空气洁净领域的探索者-CAE(Clean Air Explorer空气洁净领域的探索者)也因此而生,
我们一直在洁净室工程领域不断探索前行,目前公司已经累积了电子、微电子、半导体、实验室、
LCD-TFT、医药、医疗、激光、印刷、光学、化学、生物、食品、化妆品、相关行业的厂房净化装修成功案例,
有系统完善的行业整体解决方案、并有整体系统服务体系为保障和丰富的实施经验。
欢迎您的咨询:18915730122(微信同号)

下一篇: 已经没有了
上一篇: 已经没有了